臭氧的医疗用途及臭氧杀死病毒的机制
臭氧水用作喷雾剂或压缩剂;并用于牙科医学、老年疾病、循环系统疾病、病毒性疾病、黄斑变性、风湿病/关节炎、感染伤口、艾滋病、非典和癌症。它还可以降低血液中的胆固醇,具有抗氧化反应,用于治疗缺氧,它可以改变静息肌肉中的氧合作用,并用于缺血综合征的补充治疗(Elvis 和 Ekta,2011 年)。已经表明,在小鼠中单次皮下注射臭氧并避免了坐骨神经的神经损伤,可以减轻神经性疼痛(Elvis 和 Ekta,2011 年)。
(a) 外周阻塞性动脉疾病:臭氧诱导糖酵解增加 ATP 和 2, 3-DPG。这导致血红蛋白的 S 形 O 2结合曲线向右移动,进而导致缺血组织中的 O 2释放。这导致在存在 GSH 的情况下H 2 O 2转化为 RBC 中的H 2 O。该反应主要负责愈合缺血组织,并且已表明即使是该疾病的 IV 期,脚趾坏死和无法忍受的疼痛也可以通过 50% 的臭氧化 AHT 延迟。臭氧还刺激 HO-1、HSP70 和 Nrf2,从而诱导抗氧化剂、核转录因子和缺氧诱导因子 - 1α(HIF - 1α)。这会诱导 VEGF、EPO 和糖酵解酶来促进细胞增殖和存活。VEGF 诱导新血管生成以增加血流,从而进一步增加 EPO 以增强氧气输送。此外,糖酵解酶促进葡萄糖的代谢以增加 NO 和 CO 的生物合成,这也增加了向缺氧组织的血流和氧气输送(Sagai 和 Bocci,2011 年)。
(b) 老年性黄斑变性:主要是中央凹的感光细胞和色素性视网膜上皮细胞死亡,导致慢性缺氧。臭氧 (AHT) 有助于增加向视网膜输送氧气( Sagai 和 Bocci,2011 年)。
(c) 糖尿病:发现臭氧可降低 HbA 1 C、CRP、非酶糖基化、醛糖还原酶活性、晚期糖化终产物和抗氧化剂-促氧化剂平衡( Sagai 和 Bocci,2011 年)。
(d) 癌症:在 Sweet 等人的一项研究中。结果表明,当尝试将臭氧和氧气混合物吹入腹膜时,可以提高接受治疗的兔子的存活率( Sagai 和 Bocci,2011 年)。
(e) 神经退行性疾病:Nrf2 和 HIF - 1α臭氧通过激活 HO-1 在神经退行性疾病中的神经保护和抑制神经炎症中起重要作用(Sagai 和 Bocci,2011 年)。
(f) 皮肤和粘膜感染:臭氧用于糖尿病足、缺血性溃疡、坏死、褥疮、脓肿、肛裂、瘘管、口疮性口炎、骨髓炎、口腔炎、外阴阴道炎和甲癣( Sagai 和 Bocci,2011 年)。
(g) 背痛和骨科疾病:30-35 岁时μg/ml臭氧直接注入椎间盘突出症对应的体间隙中心,溶解在髓核水中,与由碳水化合物和多肽链组成的大分子糖蛋白(蛋白聚糖、胶原蛋白II和IV)发生反应。这会产生 OH-它重新吸收水解产物和游离水,从而导致细胞核收缩和突出物质消失(Sagai 和 Bocci,2011 年)。
臭氧杀死病毒的机制
臭氧破坏病毒蛋白、脂蛋白、脂质、糖脂或糖蛋白,使它们容易受到氧化作用并参与氧化还原反应。它还破坏病毒包膜糖蛋白和 peplomers,这对于病毒与宿主受体的附着是必不可少的。冠状病毒的刺突蛋白和包膜蛋白中含有半胱氨酸残基(Rowen 和 Robins,2020 年)。这些半胱氨酸残基由称为硫醇基 (R-SH) 的巯基组成。如病毒结构中所述,这些在病毒中处于还原状态的硫醇基团在病毒进入和病毒膜与宿主细胞膜融合中起关键作用。因此,当臭氧与这些硫醇基/巯基反应时,会将它们氧化成磺酸残基(R-SO 3-H) 如图图 3 (Fernández-Cuadros 等人,2020 年)。这个过程可以在更高的温度下得到加强。臭氧通过改变这些半胱氨酸残基使病毒的生长速度比野生型病毒低 2 log(Rowen 和 Robins,2020 年)。此外,冠状病毒具有半胱氨酸依赖性木瓜蛋白酶(一种半胱氨酸依赖性蛋白酶),该木瓜蛋白酶被氧化并降解为磺酸盐/磺酸。
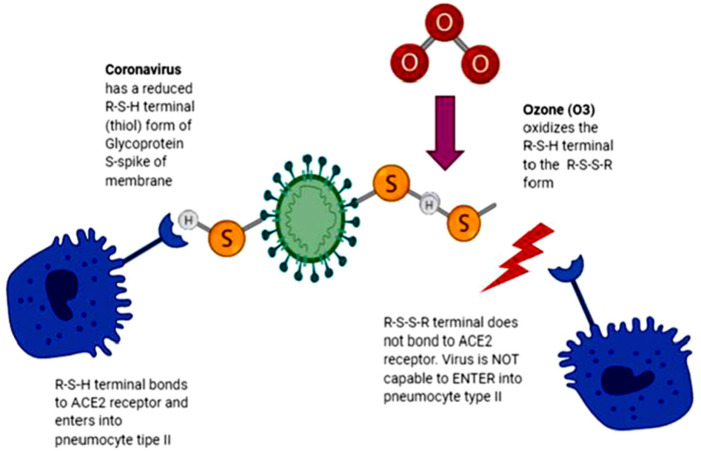
图 臭氧防止 S-spike 蛋白残基与 ACE2 受体结合的机制(Fernández-Cuadros 等人,2020 年)。
刺突蛋白还含有可被臭氧降解的色氨酸(Rowen 和 Robins,2020 年,Fernández-Cuadros 等人,2020 年)。臭氧掺入人体血清中会产生具有抗病毒作用的脂质和蛋白质过氧化物。臭氧还足以显着改变病毒包膜和病毒基因组,从而导致非致病性功能失调病毒。这些减毒病毒有助于引发对特定病毒的各种毒株的独特免疫反应,从而产生宿主特异性自身疫苗(de Wit et al., 2016 , Bocci, 1992)。除了在体内产生对任何病毒本身作出反应的抗体外,它还会产生许多高活性形式的臭氧。因此,臭氧的添加从根本上增强了宿主对病毒感染的抗原抗体反应(Di Paolo 等人,2004 年)。